Definisjon
Lupus nefritt er revmatisk nyre-betennelse (ikke infeksjon) i nyrevevets filtersystem (glomeruli) som typisk forekommer ved systemisk lupus erythematosus (SLE). Proteiner (eggehvite) og røde blodlegemer vises i urinen (hematuri) og alvorlighetsgraden bestemmes ut ifra en vevsprøve (biopsi) fra nyrene. Uten behandling fører lupus nefritt til høyt blodtrykk og livstruende nyresvikt. Oppfølging bør gjøres av leger med erfaring på lupus nefritt og i samarbeid med nyrespesialist. Best mulig behandling av lupus nefritt er viktig for best mulig prognose ved SLE (referanse: Reppe Moe SE, 2019).
Årsaker
Data fra forskning tyder på at immunsystemet mangler evnen til å fjerne døende celler (apoptose) effektivt nok. Cellekjerner som inneholder DNA stimulerer dermed immunsystemet som blir for aktivt. Ved en feil (tap av toleranse for eget vev) angriper immunsystemet vevet i kroppens egne organer. Det dannes immunkomplekser og betennelse/inflammasjon. Pasienter med DNA- eller C1q –antistoff er spesielt utsatt for en slik nyrebetennelse (glomerulonefritt). Referanse: Borchers AT, 2012
Forekomst
Ved SLE får 30-50 % nefritt. Tidlig SLE-diagnose og behandling reduserer risikoen.
Symptomer
Lupus nefritt gir ingen symptomer i tidlige sykdomsfaser, men blir påvist ved urintest og vevsprøve (biopsi).
- Mistenk lupus nefritt ved eggehvite/proteiner i urinen (stiks og mer enn 200 mg/24 timer), hematuri (røde blodlegemer i urinen), stigende blodtrykk eller redusert nyrefunksjon med stigende kreatinin og fallende GFR i blodprøver.
- Tap av proteiner via urinen over tid fører til lavt proteinnivå i blodet og vannansamlinger (ødemer) på legger og føtter oppstår.
Undersøkelser
Legen måler protein/kreatinin ratio og kvantifisering av proteiner i urin-prøve, vurder om ødemer f oreligger, måler blodtrykk og undersøker andre tegn på SLE-aktivitet (hud, ledd, hjerte).
Nefrotisk syndrom. Total proteinutskillelse. Mer enn 3g/dag i urin + ødemer og lavt albumin i blodet. Manifest glomerulær nyresykdom: Protein/Kreatinin) ratio mer enn 300.
- Normal proteinuri : opptil 150 mg/døgn
- Proteinuri mellom 30-300 mg/døgn regnes som mikroalbuminuri (normal urin-stiks)
- Patologisk proteinuri 300-500 mg/døgn
- Urin-stiks måler albuminuri pr liter :
- 1+ tilsvarer 300-1000 mg/liter
- 2+ tilsvarer 1000-3000 mg/liter
- 3+ tilsvarer mer enn 3000 mg/liter
- Ved mikroalbuminuri er urin-stiks normal
DNA antistoff og C1q antistoff disponerer for SLE-nefritt.
Graden av blod og proteiner i urin og nedsatt GFR (nyrefunksjon) korrelerer dårlig med alvorlighetsgraden av nefritt. Biopsi er derfor ofte nødvendig.
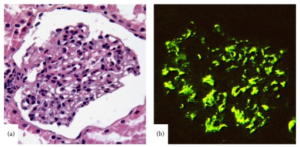
Nyrebiopsi ved SLE. Nyrebiopsi er viktig for å vurdere sykdomsaktivitet, adekvat behandling og prognose og anbefales når det er holdepunkter for nyre-manifestasjon (referanse: Fanouraiakis A, 2019 (EULAR-anbefalinger). Biopsimaterialet legges på formalin for lysmikroskopi og immunfluorescens. I tillegg legges vev på 2% glutalaldehyd for elektronmikroskopi.
- Komplikasjonsrate 2-5%
- Etter biopsi blir pasienten overvåket i 24 timer (blødningsfare). Forbigående blod i urinen (hematuri) forekommer hos 60-80%. Ultralydkontroll aktuelt
- Kontra-indikasjoner som gjør at nyre-biopsi ikke skal gjøres (referanse: Bandari J, 2016)
- Økt blødningsfare
- Ukontrollert høyt blodtrykk
- Bare en nyre
SLE nefritt klassifisering etter WHO (Grande & Balow, Lupus 1998; 611-7). Weening JJ, 2004
| Klasse 1. | Normal/Minimal mesangial (lupus)nefritt*. Forekomst <1% | |
| Klasse 2: | Mesangial proliferativ (lupus)nefritt*. Forekomst 26% | |
| Klasse 3 | Fokal proliferativ (<50% affiserte glomeruli). Forekomst 18%. Mindre enn 50% av glomeruli angrepet | |
| Klasse 4 | Diffus proliferativ (>50% affiserte glomeruli). Forekomst 38%. Mer enn 50% av glomeruli angrepet | |
| Klasse 5: | Membranøs (lupus)nefritt*, Forekomst 16% | |
| Klasse 6: | Kronisk nefritt (80% av glomeruli affisert) Sklerose, Forekomst 2%. Mer enn 90% av glomeruli angrepet | |
| *betegnes som lupus-nefritt dersom SLE foreligger |
Beskrivelse/Nomenklatur ved nyrebiopsi
- Hyper-cellularitet (fra celler i glomeruli som endotel, epitel og mesangiale celler)
- Wire-loop er eosinofil fortykkelse av glomerulus basalmembran
- Kroniske lesjoner: Dårligst prognose. Tolkes etter antall glomeruli funnet: 10% glomeruli tilsier 35% sjanse for at ingen lesjoner påvises. 20% Glomeruli: 12% sjanse for å overse affeksjon. Mange har både proksimal og distal tubulær dysfunksjon. Graden av interstitiell nefritt korrelerer best med redusert nyrefunksjon
- Segmentale forandringer betyr at bare en del av glomerulus er affisert og at heller ikke alle glomeruli har forandringer
- Halvmåne-dannelse er synonym med ekstrakapillær proliferasjon. Cellene kommer fra parietale del av Bowmans kapsel. Nekrose er neutrofile infiltrater med karyorrhexis, fibrin eksudater og diskontinuiteter i basalmembranen IgG, IgM, C1q og C3 utfelling
- Hematoksylin legemer er dannet av degenerert materiale fra cellekjernen, sees hos bare 25%, men diagnostisk for SLE
- Elektronmikroskopi: electron dense structures (EDS) i mesangium, subendotelial, subepitelial
- Podocytopati (referanse: Singh L, 2015) er en gruppe nyresykdommer som angriper celler med lange tynne utløpere (podocytter) og som deltar i filtrering av urin i nyre-glomerulum.
- Generelt den vanligste årsak til proteiner i urinen
- Kan være assosiert med SLE, men ikke nødvendigvis
- Minimal change nefropati
- Diffus mesangial sklerose
- Fokal segmantal glomerulosklerose
Behandling av moderat-alvorlig aktiv lupusnefritt
Behandlingens hensikt er å redusere risiko for endestadium av nyresvikt, samt å redusere dødelighet av sykdommen.
Behandlingen vil alltid være individuell, basert på sykdommens alvorlighetsgrad, pasientens alder og generelle tilstand, samt pasientens ønsker. Man begynner med induksjonsbehandling for å stanse betennelsen. Etter 3-6 måneder er sykdommen ofte i en rolig fase (remisjon), og en kan gå over til mildere vedlikeholdsbehandling (referanse: Fanouraiakis A, 2019)
Det finnes flere behandlingsregimer.
- Methylprednisolon iv (Solu-Medrol) 750 mg/dag i 3 dager (lavere dose i noen tilfeller, individuell tilpasning)
- Cyclofosfamid (Sendoxan) iv 500mg (eller 7,5mg/kg) hver 14.dag i 3 måneder (EURO-Lupus protokoll)
- Etter 3 måneder: Overgang til azathioprin (Imurel) 2 – 2,5 mg/kg/dag eller mykofenolat (CellCept, Myfortic) 1 -2 g/dag
- Alternativ til cyclofosfamid:
- Mykofenolat (CellCept, Myfortic) 1 – 3 g/dag (forsiktighet ved lav nyrefunksjon)
- Takrolimus (Prograf) er et alternativ hvis ikke mykofenolat kan brukes. Ved alvorlig forløp kan takrolimus kombineres med Mykofenolat (forsiktighet ved lav nyrefunksjon)
- Prednisolon
- Uke 1-4 Prednisolon 20 mg/dag
- Uke 5-6 Prednisolon 15 mg/dag
- Uke 7-8 Prednisolon 10 mg/dag
- Uke 9-10 Prednisolon 7,5 mg/dag
- Uke 11- 6 måneder Prednisolon 5 mg/dag
- Etter ett år: Vurdere å avslutte Prednisolon
Ved nefrotisk syndrom og lavt albumin i serum foreligger økt risiko for tromboembolier. Vurder antitrombotisk behandling
- Antifosfolipid syndrom (APLS) forekommer hos noen med Lupus og kan i seg selv gi nyre/blodåre komplikasjoner
Få kontroll på proteinuri som er viktig prognostisk faktor, samt redusere hematuri og stabilisere GFR
- Anti-proteinuri-behandling med ACE hemmer (for eksempel enalapril/Renitec) eller AT-II hemmer (for eksempel losartan/Cozaar)
- Etter påbegynt behandling forventes proteinuri å nå stabilt og lavt eller fraværende nivå etter 18 måneder
- Etter 3-4 måneder forventes målbar behandlingseffekt
- Manglende virkning etter 6-12 måneder oppfattes som delvis manglende behandlingseffekt
- Hvis ikke effekt etter 24 måneder mangler en komplett respons
Etter induksjonsbehandling av lupus nefritt anbefales minst tre år påfølgende immunsupprimerende behandling
Behandlingsalternativer ved manglende behandlingseffekt (behandlingsresistente tilfeller)
- Hvis Sendoxan (cyklofosfamid intravenøst) ikke har tilstrekkelig effekt, vurderes bytte til mykofenolat (CellCept tabletter) 2-3 g/døgn
- Hvis mykofenolat (CellCept) ikke virker, vurderes bytte til Sendoxan
- Hvis verken Sendoxan eller CellCept virker, kan rituksimab (MabThera) overveies
- Takrolimus har sammenlignbar effekt som mykofenolat som induksjonsterapi (Mok CC, 2020)
- Et alternativ i behandlingsresistente tilfeller er å kombinere CellCept (1-2g/d) med Takrolimus (4mg/kg/d hos voksen person) (referanser: Liu Z, 2015 (induksjonsbehandling); Zhang H, 2017 (vedlikeholdsbehandling)
- Prednisolon kontinueres og trappes ned over tid. Initialt kan intravenøs metylprednisolon (SoluMedrol) 500mg iv overveies (for eksempel tre dager på rad).
Litteratur
- Norby GE, 2010 (Tidsskriftet)
- Fanouraiakis A, 2019 (EULAR-anbefalinger)
- Wilhelmus S, 2016
- Kronbichler A 2013: Renal involvement in autoimmune CTDs
- Aasarød K, 2016 (oversikt over glomerulonefritt-sykdommer)
- Ruiz-Irastorza G, 2010 (Plaquenil-anbefalinger)

